راهنمای ۲۰۲۳ برای تشخیص و مدیریت فیبریلاسیون دهلیزی: دیدگاههای کلیدی
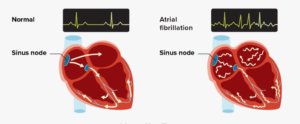
در ادامه دیدگاههای کلیدی از راهنمای ۲۰۲۳ ACC/AHA/ACCP/HRS برای تشخیص و مدیریت فیبریلاسیون دهلیزی (AF) ارائه شده است:
- طبقهبندی فعلی دستورالعمل AF بر مراحل AF از جمله دوره پیش از تشخیص تمرکز دارد. مرحله ۱: در معرض خطر AF (وجود عوامل خطر قابل تغییر و غیرقابل تغییر)، مرحله ۲: پیش از AF (شواهد یافتههای ساختاری یا الکتریکی مستعدکننده AF)، مرحله ۳A: AF حملهای (متناوب، تا ۷ روز طول میکشد)، مرحله ۳B: AF پایدار (مداوم و بیش از ۷ روز ادامه دارد و نیاز به مداخله دارد)، مرحله ۳C: AF پایدار طولانیمدت (AF مداوم که بیش از ۱۲ ماه طول میکشد)، مرحله ۳D: ابلیشن موفق AF (بدون AF پس از ابلیشن یا مداخله جراحی)، و مرحله ۴: AF دائمی (عدم تلاش بیشتر برای کنترل ریتم). کنترل زودهنگام ریتم با احتمال بیشتر حفظ ریتم سینوسی در درازمدت و به حداقل رساندن بار AF و کاهش پیشرفت بیماری مرتبط است.
- تغییر سبک زندگی و عوامل خطر، ستون اصلی مدیریت AF برای جلوگیری از شروع، پیشرفت و پیامدهای نامطلوب است. برای بیماران مبتلا به AF، این دستورالعمل توصیه میکند: ۱) کاهش وزن در افراد با شاخص توده بدنی بالای ۲۷ کیلوگرم بر متر مربع، ۲) تمرین ورزشی با شدت متوسط تا شدید با هدف ۲۱۰ دقیقه در هفته، ۳) ترک دخانیات، ۴) به حداقل رساندن یا حذف مصرف الکل، ۵) کنترل بهینه فشار خون، و ۶) غربالگری برای اختلالات تنفسی مرتبط با خواب.
- این دستورالعمل استفاده از یک امتیاز خطر بالینی معتبر مانند CHA2DS2-VASc، ATRIA یا GARFIELD-AF را تأیید میکند. بیماران مبتلا به AF با خطر سالانه متوسط حوادث ترومبوآمبولیک (کمتر از ۲%) ممکن است از در نظر گرفتن عوامل اضافی که ممکن است خطر سکته مغزی آنها را تغییر دهد، بهرهمند شوند: بار بیشتر AF، AF پایدار یا دائمی در مقابل حملهای، چاقی، کاردیومیوپاتی هیپرتروفیک، فشار خون بالا با کنترل ضعیف، نرخ فیلتراسیون گلومرولی تخمینی (کمتر از ۴۵ میلیلیتر بر ساعت)، پروتئینوری (بیشتر از ۱۵۰ میلیگرم بر ۲۴ ساعت)، حجم دهلیز چپ بزرگشده (بیشتر یا مساوی ۷۳ میلیلیتر) یا قطر (بیشتر یا مساوی ۴.۷ سانتیمتر).
- امتیازات خطر خونریزی نباید به تنهایی برای تعیین واجد شرایط بودن برای داروهای ضد انعقاد خوراکی (OAC) استفاده شوند، بلکه باید برای شناسایی و اصلاح عوامل خطر خونریزی و اطلاعرسانی در تصمیمگیری پزشکی به کار روند. در بیماران مبتلا به AF که خطر سالانه تخمینی سکته مغزی یا حوادث ترومبوآمبولیک آنها ≥۲٪ است، درمان برای کاهش خطر سکته مغزی باید بر اساس خطر ترومبوآمبولیسم باشد، چه الگوی AF حملهای باشد، چه پایدار، پایدار طولانیمدت یا دائمی. داروهای ضد انعقاد خوراکی مستقیم به جز در بیماران مبتلا به تنگی میترال یا دریچههای مکانیکی قلب، بر وارفارین ترجیح داده میشوند. در بیماران مبتلا به AF که کاندیدای ضد انعقاد هستند و هیچ نشانهای برای درمان ضد پلاکتی ندارند، آسپرین به تنهایی یا در ترکیب با کلوپیدوگرل به عنوان جایگزینی برای ضد انعقاد برای کاهش خطر سکته مغزی توصیه نمیشود. در بیماران مبتلا به AF و بیماری عروق کرونر مزمن (بیش از ۱ سال پس از رگگشایی یا بیماری عروق کرونر که نیاز به رگگشایی کرونر ندارد) بدون سابقه ترومبوز استنت، مونوتراپی OAC بر درمان ترکیبی OAC و یک عامل ضد پلاکتی (آسپرین یا مهارکننده P2Y12) برای کاهش خطر خونریزی عمده توصیه میشود.
- در بیماران مبتلا به AF علامتدار که داروهای ضد آریتمی در آنها بیاثر، منع مصرف، غیرقابل تحمل یا نامطلوب بودهاند، ابلیشن کاتتر برای بهبود علائم مفید است. در بیماران منتخب (معمولاً جوانتر با بیماریهای همراه کم) مبتلا به AF حملهای علامتدار، ابلیشن کاتتر به عنوان درمان خط اول برای بهبود علائم و کاهش پیشرفت به AF پایدار مفید است. در بیماران (غیر از جوانتر با بیماریهای همراه کم) مبتلا به AF حملهای یا پایدار علامتدار که با استراتژی کنترل ریتم مدیریت میشوند، ابلیشن کاتتر به عنوان درمان خط اول میتواند برای بهبود علائم مفید باشد. ابلیشن کاتتر در بیماران AF مناسب مبتلا به نارسایی قلبی با کسر جهشی کاهشیافته توصیه میشود.
- با توجه به مطالعات اخیر، توصیههای دقیقتری برای بیماران مبتلا به AF شناساییشده توسط دستگاه (دستگاههای قابل کاشت و پوشیدنی) ارائه شده است. برای بیماران با یک دوره ضربان دهلیزی با سرعت بالا (AHRE) که توسط دستگاه شناسایی شده و ≥۲۴ ساعت طول میکشد و دارای امتیاز CHA2DS2-VASc برابر با ۲ یا خطر سکته مغزی معادل آن هستند، شروع OAC در چارچوب تصمیمگیری مشترک که مدت زمان دوره و خطر فردی بیمار را در نظر میگیرد، منطقی است. برای بیماران با یک AHRE شناساییشده توسط دستگاه که بین ۵ دقیقه تا ۲۴ ساعت طول میکشد و دارای امتیاز CHA2DS2-VASc ≥۳ یا خطر سکته مغزی معادل آن هستند، شروع ضد انعقاد در چارچوب تصمیمگیری مشترک که مدت زمان دوره و خطر فردی بیمار را در نظر میگیرد، ممکن است منطقی باشد. بیماران با یک AHRE شناساییشده توسط دستگاه که <۵ دقیقه طول میکشد و بدون هیچ نشانه دیگری برای OAC هستند، نباید OAC دریافت کنند.
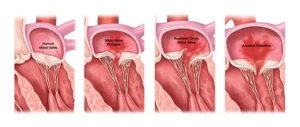
- دستورالعمل فعلی به دستگاههای انسداد زائده دهلیز چپ (LAAO) یک سطح بالاتر از توصیه (Class of Recommendation) اختصاص میدهد. در بیماران با امتیاز CHA2DS2-VASc ≥۲ و منع مصرف برای OAC طولانیمدت، انسداد زائده دهلیز چپ از طریق پوست (pLAAO) منطقی است (کلاس ۲a). در بیماران با خطر متوسط تا بالای سکته مغزی و خطر بالای خونریزی عمده در حین مصرف OAC، pLAAO ممکن است یک جایگزین منطقی برای OAC باشد (کلاس ۲b).
- در بیماران مبتلا به AF که در شرایط بیماری حاد پزشکی یا جراحی شناسایی میشوند، پیگیری سرپایی برای طبقهبندی خطر ترومبوآمبولیک و تصمیمگیری در مورد OAC، و همچنین نظارت بر AF، با توجه به خطر بالای عود AF میتواند مفید باشد. در بیماران مبتلا به AF که در شرایط بیماری بحرانی ناشی از سپسیس شناسایی میشوند، مزایای ضد انعقاد در طول بیماری بحرانی برای پیشگیری از سکته مغزی نامشخص است.
https://www.jacc.org/doi/10.1016/j.jacc.2023.08.017?_ga=2.6935730.1491959966.1723906816-2088920783.1722508824